特長 サ-ビスフロー 製造工程イメージ 価格・納期 お問い合わせ 関連サービス
特徴
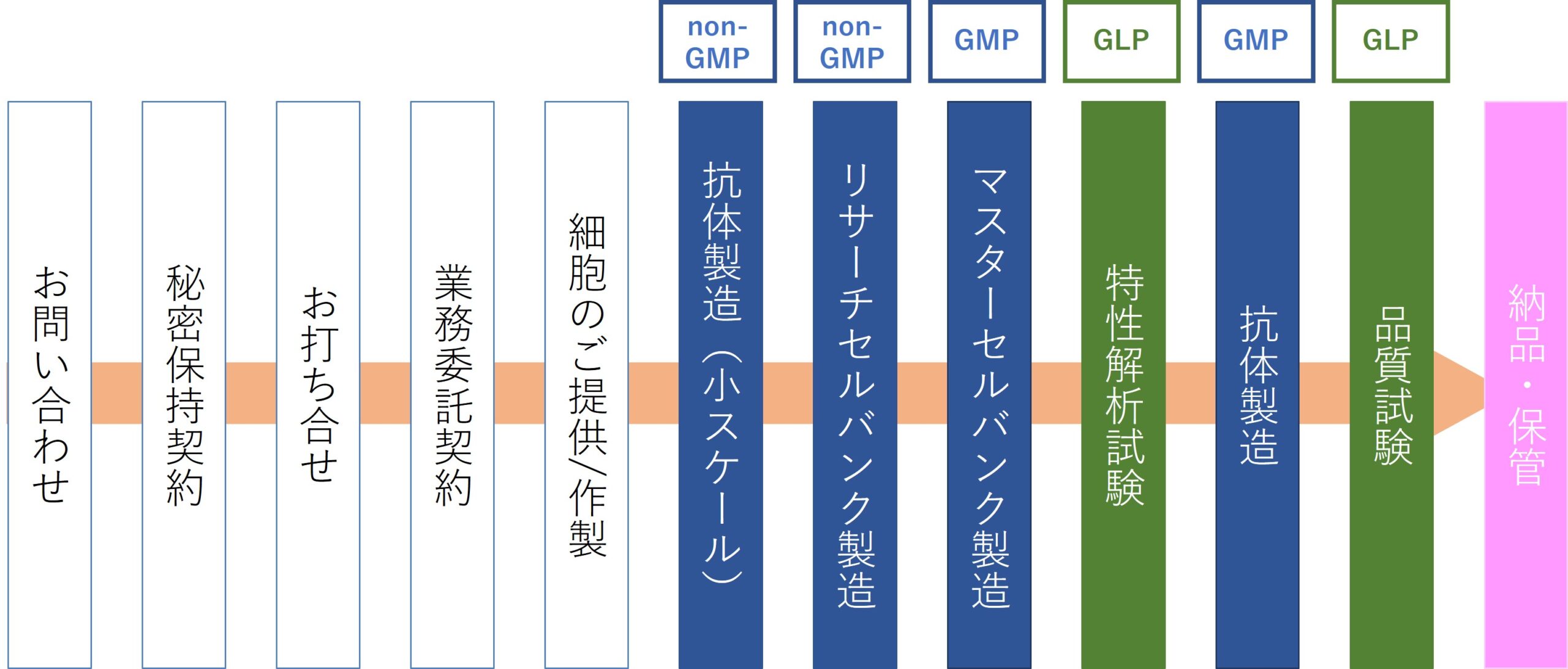
サービスフロー
製造工程イメージ
抗体製造までの流れ
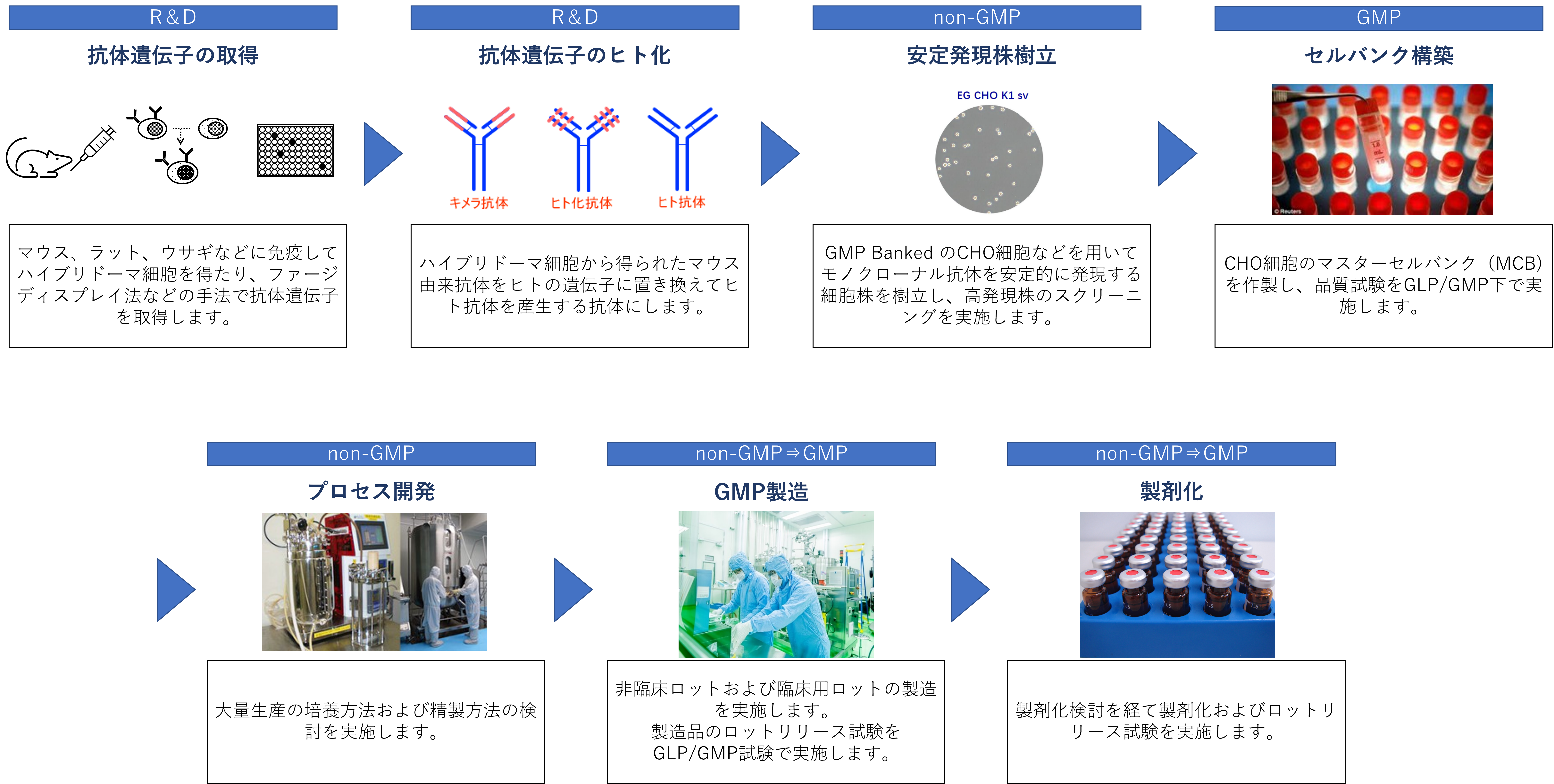
抗体医薬品製造のフロー例
プロセス開発

- 細胞製造
- 細胞培養法開発
- 精製方法開発
分析

- 純度、不純物、活性測定
- 分析方法開発
- バリデーション
- タンパク質特性解析
cGMP製造

- 各種セルバンク製造
- バイオ的手法による製造
- 品質管理(QC,QAU)
- PIC/S GMP基準でのプロジェクトマネジメント
コンジュゲーション

- 化学物質と抗体の結合
- 生物学的なコンジュゲーション作業
- ADCの分析技術
cGMPモノクローナル抗体製造施設
特徴1EirGenix社独自のEG CHO K1 sv 細胞とpEG発現ベクターをお客様の製造にご利用頂けます。
 |
|
 |
|
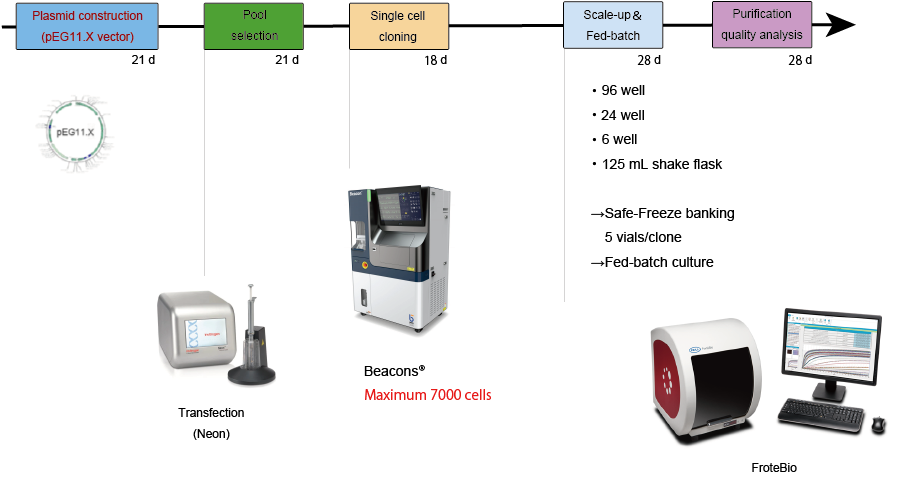
特徴2独自の発現細胞の構築システムを保有し、高い生産性を確保。
・プラスミド構築から培養精製をして高発現細胞のセレクションまで約4ヶ月~
・クローンによりますが、1g∼5g/Lの発現実績があります。
EirGenix社について
・1984年に特定非営利活動法人DCB*(Development Center for Biotechnology)のバイオ医薬品パイロット製造部門として設立
・2013年にDCBから独立し、EirGenix, Inc.設立
・従業員数は約340名で、2022年末には500名になる予定 約75%が Ph.D.,またはM.S.を保有
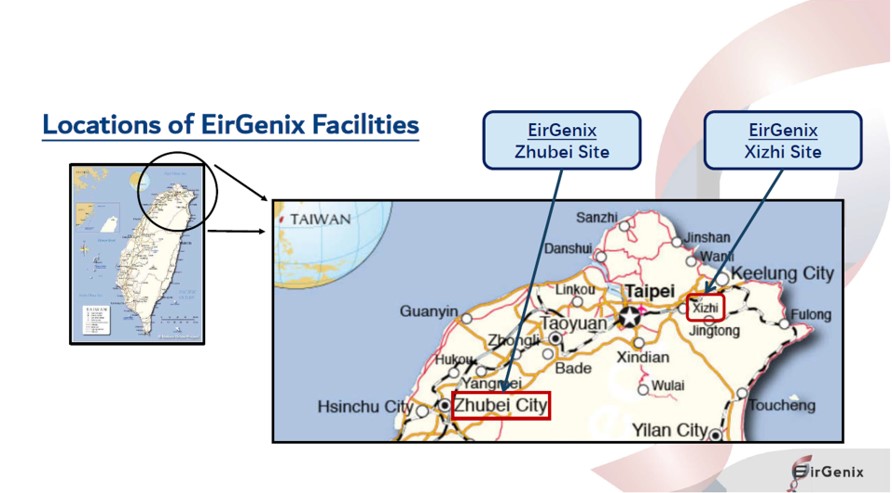
・台湾の台北新北市(汐止区:Xizhi)に本社・CDMO施設があり、竹北市(Zhubei)にも大規模なCDMO施設を2019年に新設した。
・2020年にPMDAの監査を完了し、医薬品製造業の業許可を取得済
・新北と竹北に製造サイトを2サイト有しており、新北にはパイロットプラント、竹北にはコマーシャルプラントがあります。
・新北のパイロットプラントでは、哺乳動物細胞 ~1,000Lスケール、大腸菌~100Lスケールの培養が可能です。
・竹北の2×2,000Lの培養槽が3セットあり、最大で12×2,000L培養まで可能になります。

竹北のコマーシャルプラントの建物
医薬品製造業 業許可証
・EirGenixは、日本の製薬企業とシェア30%を持つがん治療薬の長期供給契約を締結しており、PMDAの監査も終了して「医薬品適合性調査結果通知書」を受領し、CDMOとして品質を保証されています。
価格・納期
どのステージからの実施か開発期間が掛かるのかなどお客様によって状況が異なりますので、詳細にお打合せの上、お見積りを作成させて頂きます。
お問い合わせ
お問い合わせフォームまたはお電話からお気軽にお問い合わせください。